お知らせ
2024年10月07日 【プレスリリース】もやもや症候群の原因遺伝子を解明!
令和 6年10月 7日
学校法人東京女子医科大学
学校法人東京女子医科大学
もやもや症候群の原因遺伝子を解明!
次世代技術で治療の新たな鍵を発見
| Point ○ もやもや病は脳の内頚動脈が進行性に狭窄・閉塞を起こし、それを補うために脳の底部にもやもやとした異常血管網を生じる難病(指定難病22)です。脳梗塞や脳出血の原因となります。 ○ ダウン症候群や神経線維腫症I型などの遺伝性疾患に併発することがあり、この場合を特に”もやもや症候群“と呼びます。 ○ 様々な遺伝性疾患に併発したもやもや症候群の患者さんを解析した結果、肺動脈性肺高血圧症の疾患遺伝子群の機能的レアバリアントが、もやもや症候群の発生にも関わることが新たにわかりました。 ○ 将来的に、有効な薬物治療法の創出につながることが期待されます。 |
【研究の背景】
もやもや病(MMD)は内頚動脈終末部の進行性狭窄・閉塞に、異常な側副血行路(もやもや血管)の代償性発達を伴う多因子疾患*です。ダウン症候群や神経線維腫症I型(NF1)等の遺伝性疾患に併発することがあり,その場合を”類もやもや病“あるいは”もやもや症候群“と呼びます(本稿では、もやもや症候群=MMSと表記します)。脳の血流低下により一過性脳虚血発作や脳梗塞を発症したり、もやもや血管の破綻で脳内出血を起こすこともある難病です。これまで、原疾患の原因遺伝子変異そのものが、MMSの発生にも関わると考えられてきました。しかし、例えばNF1の患者さんでMMSを発生するのはごく一部にすぎません(約6%)。そのため、原疾患の原因遺伝子変異にプラスして何らかの遺伝的修飾因子が組み合わさるとMMSが発生するのではないか、と考えられるようになってきました。
【研究方法】
本研究では、アジア人・欧州人のMMS患者さん計13例(ダウン症:3例、NF1:6例、ヌーナン症候群:1例、HbH型サラセミア:1例、多系統平滑筋機能不全症候群:2例)を対象に全エクソーム解析**を行いました。まず原疾患の遺伝子診断を確定させた後、MMSの発生に関わる修飾因子を探索しました。
【研究成果】
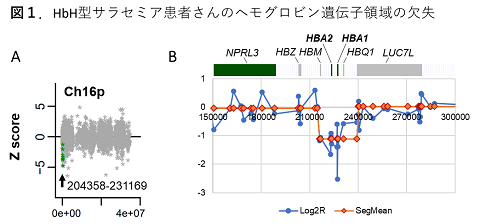
全13例で原疾患の発症に関わる遺伝子異常を特定できました。人工知能等の情報解析技術が有効にはたらき、スプライシングの異常を来す変異や、染色体領域レベルでの増幅や欠失も精度よく検出することができました。全エクソーム解析では、基本的には点変異や小さな欠失・挿入変異を検出するのが主な目的となりますが、リードのマッピングデータを有効に活用して情報解析することで比較的大きな規模の構造変異も検出することが可能です(図1)。
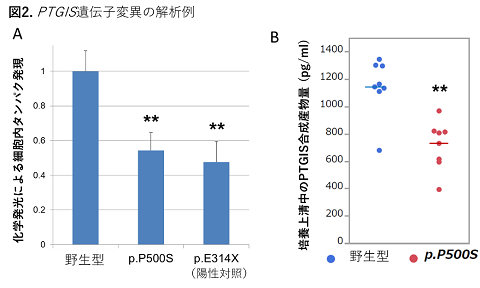
次いで、修飾因子の探索を行いました。その結果、MMD自体の感受性遺伝子バリアント、およびMMS基礎疾患遺伝子群(MM遺伝子群)の低機能バリアント**が修飾因子となり得ることが判明しました。このようなMM遺伝子群バリアントは患者群では53.8%みられたのに対し、一般人口対照では16.7%でした(P=0.003、フィッシャーの正確検定)。さらに、今回新たに見つかったのが肺動脈性肺高血圧症の遺伝子群(PAH遺伝子群)との関連です。肺動脈性肺高血圧症(PAH)は、心臓から肺に血液を送る動脈(肺動脈)の一部が狭窄する疾患で、もやもや病において脳血管でみられる病態とも類似します。また、MMDの最も有名な感受性遺伝子RNF213はPAHの疾患遺伝子でもあります。PAH遺伝子群の機能的バリアントは患者群で38.2%みられたのに対し、一般人口対照では12.0%でした(P=0.015)。MM遺伝子群で検出されたものは低機能バリアントであったのに対して、PAH遺伝子群から検出されたバリアントのうち4つでは(ABCC8: c.4412-2A>G、SMAD9:p.E30K、BMPR2:p.M356I、PTGIS: p.P500S)、培養細胞による機能解析実験により著明な機能低下が認められました(図2)。
 【今後の展望】
【今後の展望】
多因子疾患*:複数の遺伝的要因に生活習慣などの環境要因が加わって起こる病気。
全エクソーム解析**:ゲノムの中でタンパク質をコードするエクソン領域を選択的に抽出して配列を解読する手法。このような領域はゲノムの約1%にすぎないが、メンデル遺伝病の原因変異の約85%が集積していると考えられているため、効率が良い。
低機能バリアント***:本稿ではHypomorphic variantの和訳として使用。遺伝子の機能を部分的に低下させるバリアント。
【謝辞】この研究はJSPS科研費 19K09537の助成を受けたものです。
全13例で原疾患の発症に関わる遺伝子異常を特定できました。人工知能等の情報解析技術が有効にはたらき、スプライシングの異常を来す変異や、染色体領域レベルでの増幅や欠失も精度よく検出することができました。全エクソーム解析では、基本的には点変異や小さな欠失・挿入変異を検出するのが主な目的となりますが、リードのマッピングデータを有効に活用して情報解析することで比較的大きな規模の構造変異も検出することが可能です(図1)。

次いで、修飾因子の探索を行いました。その結果、MMD自体の感受性遺伝子バリアント、およびMMS基礎疾患遺伝子群(MM遺伝子群)の低機能バリアント**が修飾因子となり得ることが判明しました。このようなMM遺伝子群バリアントは患者群では53.8%みられたのに対し、一般人口対照では16.7%でした(P=0.003、フィッシャーの正確検定)。さらに、今回新たに見つかったのが肺動脈性肺高血圧症の遺伝子群(PAH遺伝子群)との関連です。肺動脈性肺高血圧症(PAH)は、心臓から肺に血液を送る動脈(肺動脈)の一部が狭窄する疾患で、もやもや病において脳血管でみられる病態とも類似します。また、MMDの最も有名な感受性遺伝子RNF213はPAHの疾患遺伝子でもあります。PAH遺伝子群の機能的バリアントは患者群で38.2%みられたのに対し、一般人口対照では12.0%でした(P=0.015)。MM遺伝子群で検出されたものは低機能バリアントであったのに対して、PAH遺伝子群から検出されたバリアントのうち4つでは(ABCC8: c.4412-2A>G、SMAD9:p.E30K、BMPR2:p.M356I、PTGIS: p.P500S)、培養細胞による機能解析実験により著明な機能低下が認められました(図2)。

今回の研究により、MMSの発症にかかわる遺伝学的なメカニズムの一端が解明されました。そのうちPAH遺伝子群については有望な治療ターゲットになりうると期待されます。既にPAHの患者さんでは疾患遺伝子をターゲットにした複数の薬剤が使用できるようになっていますが、これまで有効な薬物治療法がなかったMMS患者さんへも適応できるかもしれません。もっと多くの患者さんでの研究により更なる知見の集積が望まれます。
【用語解説】
多因子疾患*:複数の遺伝的要因に生活習慣などの環境要因が加わって起こる病気。
全エクソーム解析**:ゲノムの中でタンパク質をコードするエクソン領域を選択的に抽出して配列を解読する手法。このような領域はゲノムの約1%にすぎないが、メンデル遺伝病の原因変異の約85%が集積していると考えられているため、効率が良い。
低機能バリアント***:本稿ではHypomorphic variantの和訳として使用。遺伝子の機能を部分的に低下させるバリアント。
【謝辞】この研究はJSPS科研費 19K09537の助成を受けたものです。
【お問い合わせ先】
<研究に関すること>
赤川 浩之(あかがわ ひろゆき)
東京女子医科大学総合医科学研究所/メディカルAIセンター/足立医療センター脳神経外科 准教授
〒162-8666 東京都新宿区河田町8-1
Tel:03-3353-8111 Fax:03-5269-7038
E-mail: akagawa.hiroyuki@twmu.ac.jp
<報道取材に関すること>
東京女子医科大学 広報室
〒162-8666 東京都新宿区河田町8-1
Tel:03-3353-8111 Fax:03-3353-6793
E-mail: kouhou.bm@twmu.ac.jp
【プレスリリース情報】
1.掲載誌名:Scientific Reports
2.論文タイトル:Whole-exome sequencing reveals the genetic causes and modifiers of moyamoya syndrome
3.著者名:中村彰一、野村俊介、原祥子1、Thiparpa Thamamongood、前原健寿1、成相直1、Shasha Khairullah2、Kay Sin Tan2、東剣虹、永井礼子3、古谷喜幸、堀貴洋、山口浩司、川俣貴一、Constantin Roder4、赤川浩之*
(*はcorresponding author、アンダーラインは本学所属の著者、1: 東京科学大学脳神経外科、2:マレーシア大学内科、3:北海道大学小児科、4:チュービンゲン大学脳神経外科)
4.DOIコード: 10.1038/s41598-024-72043-5
5.論文のオンライン掲載日 :2024年10月4日
<研究に関すること>
赤川 浩之(あかがわ ひろゆき)
東京女子医科大学総合医科学研究所/メディカルAIセンター/足立医療センター脳神経外科 准教授
〒162-8666 東京都新宿区河田町8-1
Tel:03-3353-8111 Fax:03-5269-7038
E-mail: akagawa.hiroyuki@twmu.ac.jp
<報道取材に関すること>
東京女子医科大学 広報室
〒162-8666 東京都新宿区河田町8-1
Tel:03-3353-8111 Fax:03-3353-6793
E-mail: kouhou.bm@twmu.ac.jp
【プレスリリース情報】
1.掲載誌名:Scientific Reports
2.論文タイトル:Whole-exome sequencing reveals the genetic causes and modifiers of moyamoya syndrome
3.著者名:中村彰一、野村俊介、原祥子1、Thiparpa Thamamongood、前原健寿1、成相直1、Shasha Khairullah2、Kay Sin Tan2、東剣虹、永井礼子3、古谷喜幸、堀貴洋、山口浩司、川俣貴一、Constantin Roder4、赤川浩之*
(*はcorresponding author、アンダーラインは本学所属の著者、1: 東京科学大学脳神経外科、2:マレーシア大学内科、3:北海道大学小児科、4:チュービンゲン大学脳神経外科)
4.DOIコード: 10.1038/s41598-024-72043-5
5.論文のオンライン掲載日 :2024年10月4日


